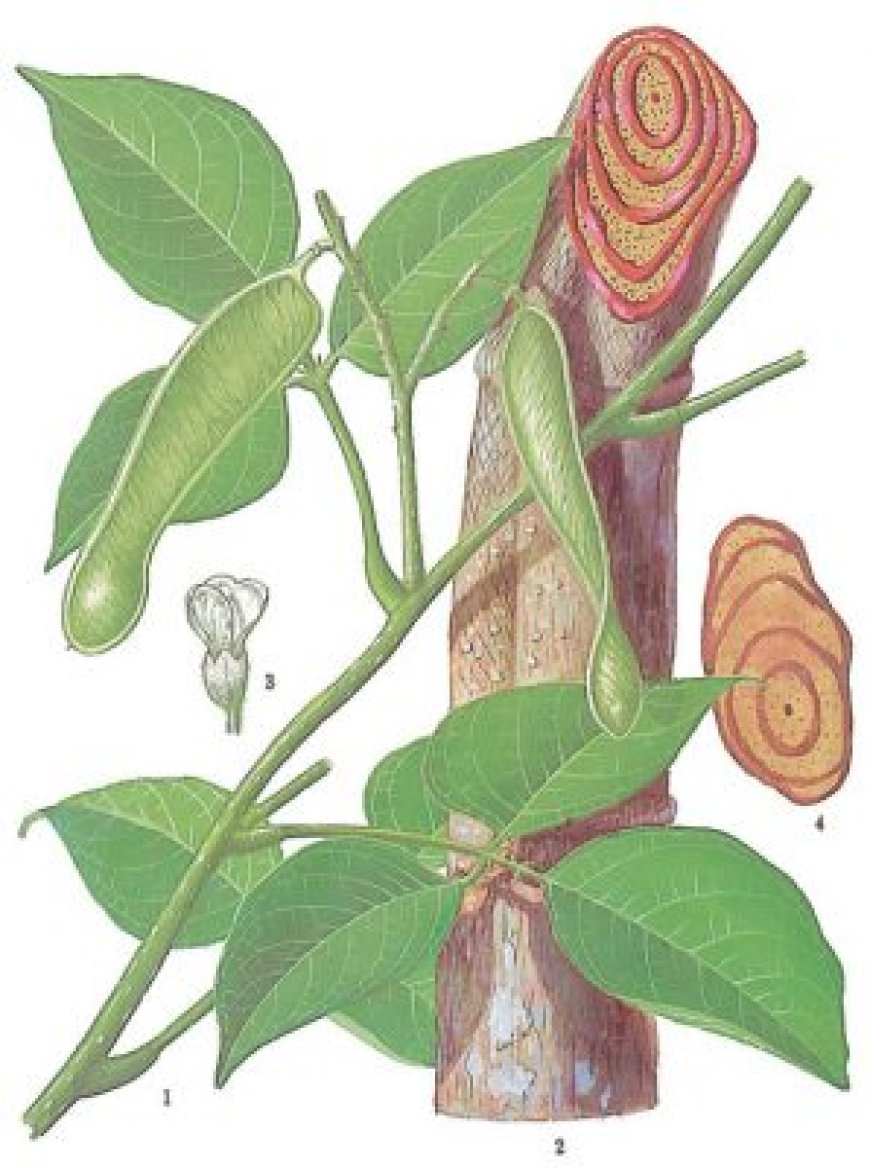
CÁC HỢP CHẤT FLAVONOID TỪ CÂY KÊ HUYẾT ĐẰNG (MILLETIA RETICULATA) Ở VIỆT NAM
Các thực vật chi Thàn mát (Millettia) với thành phần hóa học chính thuộc nhóm flavonoid được biết đến là các dược liệu quý và đã được ứng dụng rất nhiều trong các bài thuốc dân gian.
Tóm tắt
Các thực vật chi Thàn mát (Millettia) với thành phần hóa học chính thuộc nhóm flavonoid được biết đến là các dược liệu quý và đã được ứng dụng rất nhiều trong các bài thuốc dân gian. Đặc biệt, loài Milletia reticulata Benth có tác dụng chữa đau nhức xương khớp, thấp khớp; trị lưng gối đau mỏi tê bại, đòn ngã tổn thương, hoạt huyết,.. Từ cặn n-hexane và ethyl acetate của thân cây Kê huyết đằng (Millettia reticulata) ở Lạng Sơn đã phân lập và xác định cấu trúc hóa học ba hợp chất flavonoid: 5-hydroxy-6,7-dimethoxyflavanone (MR1), 4′-methoxytectochrysin (MR2) và pashanone (MR3). Cấu trúc hóa học của chúng đã được làm sáng tỏ bằng phổ cộng hưởng từ hạt nhân 1 chiều và hai chiều, kết hợp so sánh với tài liệu tham khảo. Kết quả này phù hợp với thành phần hóa học chính của các loài thuộc chi Millettia đã công bố.
Từ khóa
Milletia, Milletia reticulata, Flavonoid; 4′-methoxytectochrysin; Pashanone
Toàn văn: Tải file đính kèm dưới bài
Tài liệu tham khảo
[1] J. T. Banzouzu, A. Prost, M. RaJemiarimiraho, and P. Ongoka, “Traditional uses of the African Millettia species (Fabaceae),” International Journal of Botany, vol. 4, no. 4, pp. 406-420, 2008.
[2] T. B. Nguyen, Fabaceae family in the List of Plants of Vietnam. Agriculture Publishing House, 2003.
[3] V. C. Vo, Dictionary of Vietnamese Medicinal Plants. Publishing House Medicine, 2012.
[4] H. B. Do, Q. C. Dang, X. C. Bui, T. D. Nguyen, T. D. Do, V. H. Pham, N. L. Vu, D. M. Pham, K. M. Pham, T. T. Doan, T. Nguyen, and T. Tran, The medicinal plants and animals in Vietnam. Science and Technology Publishing House, 2004.
[5] J. W. Kamau, “Phytochemistry and Biological activity of the root extract of Millettia oblata,” Degree Master of Science (Medicinal Chemistry), Jomo Kenyatta University of Agriculture and Technology, 2002.
[6] A. C. Rana and B. Gulliya, “Chemistry and Pharmacology of Flavonoids- A Review,” Indian Journal of Pharmaceutical Education and Research, vol. 53, no. 1, pp. 8-20, 2019.
[7] T.-Y. Wang, Q. Li, and K.-S. Bi, “Review-Bioactive flavonoids in medicinal plants: Structure, activity and biological fate,” Asian Journal of Pharmaceutical Sciences, vol. 13, no. 1, pp. 12-23, 2018.
[8] S.-C. Fang, C.-L. Hsu, H.-T. Lin, and G.-C. Yen, “Anticancer Effects of Flavonoid Derivatives Isolated from Millettia reticulata Benth in SK-Hep-1 Human Hepatocellular Carcinoma Cells,” Journal of Agricultural and Food Chemistry, vol. 58, no. 2, pp. 814-820, 2010.
[9] K. P. P. Nguyen, Methods for isolating organic compounds. National University Ho Chi Minh City Publishing House, 2007.
[10] D. T. Nguyen, The basis of spectral methods applied in chemistry. Science and Technics Publishing House, 2011.
[11] D. T. Nguyen, Spectroscopic methods in organic chemistry. Hanoi National University Publishing House, 2010.
[12] T. T. T. Tran, D. Q. Tran, T. H. A. Nguyen, and V. S. Tran, “Chemical constituents of Miliusa sinensis Finet et Gagnep. (Annonaceae). Part 1 – Flavonoides,” Vietnam Journal of Chemistry, vol. 47, no. 6, pp. 745-748, 2009.
[13] H. Yoon, S. Eom, J. Hyun, G. Jo, D. Hwang, S. Lee, Y. Yong, J. C. Park, Y. H. Lee, and Y. Lim, “1H and 13C NMR Data on Hydroxy/methoxy Flavonoids and the Effects of Substituents on Chemical Shifts,” Bull. Korean Chem. Soc., vol. 32, no. 6, pp. 2101-2107, 2011.
[14] J. C. Romero-Benavides, G. C. Ortega-Torres, J. Villacis, S. L. Vivanco-Jaramillo, K. I. Galarza-Urgilés, and N. Bailon-Moscoso, “Phytochemical Study and Evaluation of the Cytotoxic Properties of Methanolic Extract from Baccharis obtusifolia,” International Journal of Medicinal Chemistry, vol. 2018, pp. 1-5, 2018, Art. no. 8908435.
[15] R. Mangoyi, J. Midiwo, and S. Mukanganyama, “Isolation and characterization of an antifungal compound 5-hydroxy-7,4’-dimethoxyflavone from Combretum zeyheri,” BMC Complement Altern Med., vol. 15, 2015, Art. no. 405.
[16] A. Hailemariam, M. Feyera, T. Deyou, and N. Abdissa, “Antimicrobial Chalcones from the Seeds of Persicaria lapathifolia,” Biochem Pharmacol (Los Angel), vol. 7, 2018, Art. no. 237, doi: 10.4172/2167-0501.1000237.
[17] C.-S. Yoon, H. Lee, Z. Liu, H.-K. Lee, and D.-S. Lee, “Effects of Compounds Isolated from Lindera erythrocarpa on Anti-Inflammatory and Anti-Neuroinflammatory Action in BV2 Microglia and RAW264.7 Macrophage,” Int. J. Mol. Sci., vol. 23, 2022, Art. no. 7122, doi: 10.3390/ijms 23137122.
[18] S. N. Lo´pez, M. G. Sierra, S. J. Gattuso, R. L. Furlan, and S. A. Zacchino, “An unusual homoisoflavanone and a structurally-relateddihydrochalcone from Polygonum ferrugineum (Polygonaceae),” Phytochemistry, vol. 67, pp. 2152-2158, 2006.
[19] A. V. Kurkina, T. Ryasanova, and K. V. Alexandrovich, “Flavonoids from the Aerial Part of Polygonum hydropiper,” Chemistry of Natural Compounds, vol. 49, no. 5, 2013, doi: 10.1007/s10600-013-0758-y.
[20] R. Kubinova, R. Porizkova, T. Bartl, A. Navratilova, A. Čizek, and M. Valentova, “Biological activities of polyphenols from Polygonum lapathifolium,” Bol Latinoam Caribe Plant Med Aromat, vol. 13, no. 6, pp. 506-516, 2014.
Các tác giả
1. Vũ Thị Thu Lê, Trường Đại học Nông Lâm – ĐH Thái Nguyên
2. Ngô Thị Trang, Học viện Khoa học và Công nghệ - Viện Hàn lâm Khoa học và Công nghệ Việt Nam
3. Nguyễn Thị Huệ, Trường Đại học Khoa học tự nhiên – ĐH Quốc gia Hà Nội
4. Lê Thị Huyền, Trường Đại học Khoa học tự nhiên – Đại học Quốc gia Hà Nội
5. Vũ Thành Đạt, Viện Hóa học các hợp chất thiên nhiên – Viện Hàn lâm Khoa học và Công nghệ Việt Nam
6. Đỗ Tiến Lâm Email to author, Viện Hoá học các hợp chất thiên nhiên - Viện Hàn lâm Khoa học và Công nghệ Việt Nam
7. Đặng Thị Ngọc Hà, Trường Đại học Nông Lâm – ĐH Thái Nguyên